استخدامات الفاناديوم واستخداماته وفقًا لحالات التأكسد الخاصة به
هذا المحتوى مأخوذ من منحة كلية Stanford Advanced Materials لعام 2025 مقدمة من أديسون بويل.
مقدمة
يُعد الفاناديوم جزءًا من المعادن الانتقالية؛ حيث يبلغ عدده الذري 23. وتبلغ نسبة وفرة الفاناديوم في القشرة الأرضية حوالي (0.02%) مماثلة للزنك.1 وعلى الرغم من وفرة الفاناديوم إلا أنهلم يحظَ باهتمام كبير حتى الخمسين سنة الماضية. أظهرت الأبحاث أن الفاناديوم يمكن أن يكون له غرض بيولوجي من خلال أيون الفانادات.2هناك ما لا يقل عن 6 حالات أكسدة مختلفة؛ حيث يوجد الفاناديوم بشكل أساسي في +3 و+4 و+5. عند عزله، تقدم كل حالة من حالات الأكسدة لونًا مختلفًا. V4+ أزرق ، و V3+ أخضر، و V2+ بنفسجي.3 هذهالأكسدة هي أيضًا الأكثر صلة بالأنظمة البيولوجية.4
الفاناديوم في الدم
تعد حالات أكسدة الفاناديوم هذه مهمة لأنها يمكن أن تمر بتفاعلات الأكسدة والاختزال.4 يعتمدالاستقرار على الربط والمذيب ودرجة الحموضة.2 من الناحية البيولوجية، وهذايعني أن هناك عوامل اختزال يمكنها تحويل الفاناديوم إلى حالات أكسدة أقل.4 تعتمد هذه العملية على درجة الحموضة،فعندما يزدادالرقم الهيدروجيني تنخفض إمكانات الأكسدة والاختزال.4 عندما يؤخذ في شكل دواء، فإنه يدخلمجرى الدم ويدخل في مكونات مصل الدم.4 ويحدد التفاعل مع الفاناديومنوع الفاناديوم.1
في ظل الظروف الحمضية المعتدلة، يشبه V(III) عند تكوينه الأنظمة البيولوجية الموجودة.1 يمكن أن تحتوي بلازما الدمعلى عوامل الاختزال الموجودة التي يمكن أن تؤدي إلى استقرار V(III) مما يسمح بتكوين أنواع V(III) 2-hTF.1هذه الأنواع تشبهFe(III) 2-hTF، والتي تتعرفعليها مستقبلاتالخلايا.1 يمكن أن يتم ذلك عندما ينجذب V(III) أو Fe(III) إلى HTF إذا كان V(IV)O في بلازما الدم متاحًا، فإن الاختزال إلى V(III) يمكن أن يكون مواتيًا من اكتساب الطاقة.1 إن ارتباط V(III) له لوغاريتم معامل تفكك V(III) 20، بينما إذا كان V(IV)O+2له لوغاريتم معامل تفكك V (IV)O+2 له لوغاريتم 13.1 يجب أن يكون هذا التفاعل في ظروف حمضية معتدلة.1
وقد لوحظ أن حالات الأكسدة الأخرى للفاناديوم (V(IV) وV(V)) يمكن أن تخضع لتبادل الروابط والتحويل البيني للأكسدة والاختزال.1 مع وجود روابط ذاتكتل جزيئية منخفضة هي اللاكتات والسترات، والكتلة الجزيئية العالية هي hTF والألبومين والغلوبولين المناعي G.1 مع كون الـ hTF هو الأكثر غلبة.1كما هو الحال في V (III)، يتفاعل V(IV) وV(V) بشكل جيد بسبب بقايا مواقع ارتباط الحديد (III) بـ hTF.1 لأن مستقبلات الخلايا الخاصة بـ hTF 2 تتعرف على الحديد (III) من خلال مستقبلات الخلاياللتخلل الداخلي.1 يمكن أن يكون هذا ممكنًا لمركبات V(IV) وV(V) أيضًا.1 عندمايتم احتضان V(IV)OSO4 و apo-hTFيتوافق مع hTF.1 كما تبين أن نسبة التكوينأقل من نسبة تكوين Fe(III) 2hTF.1وقد لوحظ أن مركبات VIVO و VIVO الناقلة، إلى جانب V(V) كأحادي الفاناديوم، قد ترتبط بـ holo-hTF، وهو العامل الناقل داخل الدم.1 بمعنى أن الفاناديوم يمكنأن يكون موجودًا في بلازما الدم ويمر عبر عملية التخلل الداخلي عندما يدخل الهولو إلى الخلايا.1
الفاناديوم
هناك 3 أنواع رئيسية من التفاعلات التي يمكن إجراؤها مع الفانادات في الكيمياء المائية: تفاعلات التكثيف الذاتي، وتفاعلات التنسيق، وتفاعلات الأكسدة والاختزال.4
بالنسبة لتفاعلات التكثيف الذاتي، يتم بروتنة أنيونات الفانادات بواسطة القِلَّات في بيئة حمضية معتدلة لجعلها أكثر ملاءمة.4 وهذا أمربالغ الأهمية لوظيفة الخلية بسبب كيفية تأثير الأس الهيدروجيني على العُضيات المختلفة.4وقد ثبت أن الخلايا السرطانية لديها أس هيدروجيني مرتفع في الخلايا السرطانية.4 وهذا قد يعني أنه يمكن استخدامالفانادات لإيجاد الخلايا السرطانية ذات الأس الهيدروجيني المرتفع.4 ويمكن القيام بذلك باستخدامسلسلة من القِلَّات من الفانادات في بيئة حمضية.4
وبما أن الفانادات له أوجه تشابه مع الفوسفات فقد بدأ استخدام الفانادات في التفاعلات التنسيقية، ولكن لا يزال معظمها في مرحلة أنابيب الاختبار، مما يعني أن معظم التفاعلات المنسقة هي تفاعلات نظرية.4 الفوسفاتمهم للأنظمة البيولوجية ويشارك في العديد من أنظمة التعرف البيولوجي والأنظمة التحفيزية الحيوية.1 حيثتتشابهمركبات الفاناداتVO43- هيكليًا وإلكترونيًا معمركب PO43- الشكل 1.4 تحتويمركبات الفانادات على هندسة هندسية خماسية الإحداثيات ثلاثية ثنائية الهرمات، مما يطابق الحالات الانتقالية خماسية الإحداثيات المفترض أن تتشكل في تفاعل الإنزيمات المعتمدة على الفوسفات الشكل 1.1 في حين أنه يمكنأن تكون هناك روابطأحادية ومتعددة الإحداثيات، فإن تلك التي تستخدم في المقام الأول هي استرات الفانادات وأنهيدريدات الفانادات، بسبب تناظرها مع الفوسفات. 4 من خلال النمذجة الحاسوبية، كان معظم الفانادات على شكل H2VO4- وH2VO42-عند استبعاد البروتينات، وعندما تم تضمين البروتينات، كان معظم الفاناديوم مرتبطًا بالترانسفيرين.4 عندما يتم تثبيتمركب الفاناداتالمعدني بواسطة الروابط، فإن هذا يزيد من فرصة الاختزال.4 وهذا يؤدي إلىتفاعلات تناسقية تميل إلى الاختزال في الأنظمة البيولوجية.4
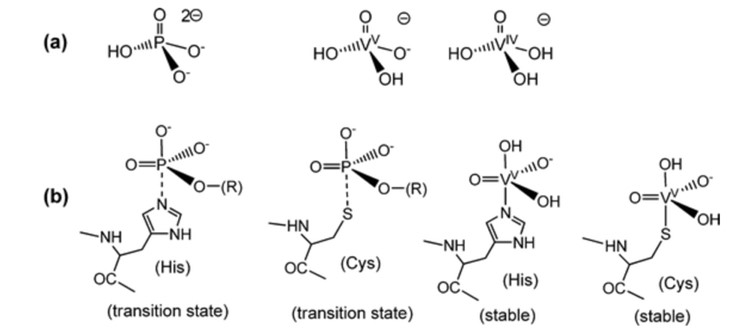
الشكل 1. مقارنة بين الفوسفات والفانادات مع حالات الانتقال والاستقرار.5
في تفاعلات الأكسدة والاختزال في الأنظمة البيولوجية، تكون حالات الأكسدة التي تخص الفاناديوم هي +3 و+4 و+5.4 معظماختزال الفانادات إلى V(IV) من V(V).4 يحدث هذا النوع من التفاعل لمجموعة متنوعة منالجزيئات الحيوية ، خاصة في العضيات.4 كما أنه يستخدم كمخزن لبروتينات الفوسفوتيروزيل.4وهذا يؤدي إلى التدخل في مسار إشارات الأنسولين.4 يمكن استخدام هذا في علاج داء السكري لأنه بمجرد ارتباطه في الموقع النشط للإنزيم، لا يتم إطلاق الفانادات بسهولة مثل الفوسفات.1 وهذايحجب الموقع عن الفوسفات، مما يؤدي إلى تثبيط الإنزيم.1 هناك عيوبلاستخدام الفانادات لعلاج داء السكري، مثل الإجهاد التأكسدي الناجم عن الفاناديوم، ومشاكل السمية العالمية، والتأثيرات على الجهاز المناعي، والالتهابات.1
أبحاث السرطان:
تم فحص خواص الفاناديوم لمعرفة تأثيراته الوقائية الكيميائية والمضادة للأورام في مكافحة السرطان.1 يبدو أنالاختبارات كانت في مراحل الاختبار على الحيوانات وعلى خطوط الخلايا الخبيثة.1ثنائي كلوريد الفانادوسين والعديد من مركبات البيروكسفانادات هي مركبات الفاناديوم الرئيسية التي تم استخدامها.1 ثنائي كلوريد الفانادوسين ثنائي كلوريد الفانادوسين قابل للذوبان في الماء، وعند درجة حموضة 7 يتم استبدال أيونات الكلوريد بـ H2O،مما يؤديإلى V(C5H5)2]2+.1وقدلوحظ أنهيرتبط بالحمض النووي، مما يسبب سلوكًا مختلفًا عن السيسبلاتين.1 كما أظهر سمية محدودة، ولا ينتقلعبر حاجز الدم، ولا يتم اكتشافه في الدماغ.1 وتتمثل أهداف الخصائص المضادة للسرطان للفاناديوم في تعطيل الأيض الخلوي ومسارات نقل الإشارات وتعطيل تكاثر الخلايا.1كانت هناك مخاوف بشأن الاستجابات المتنوعة وسلامة الفاناديوم، مما أدى إلى نقص في الأبحاث السريرية.1 مع أخذ هذه المخاوف فيالاعتبار لا يزالالناس يقومون بالأبحاث.1 تم اختبار أنظمة V(V)-mhcpe في المختبر وتم الحصول على نتائج تفيد بأنها أكثر سمية للخلايا السرطانية من الخلايا غير السرطانية.1 أظهرت مجمعات V(IV)التي تحتوي على مشتقات 1-10-فينانثرولين كروابط ومجمعات V(IV)O-dppz خصائص مضادة للسرطان الشكل 2، خاصة ضد سرطان الدم.1
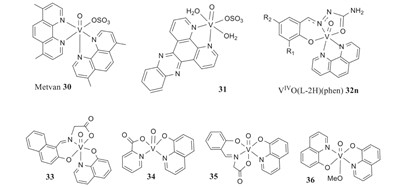
الشكل 2. تصوير المركبات المضادة للورم لمركبات الفانادات، مع ثبات الأس الهيدروجيني 7.1
أمافادين
يوجد فطر يتراكم فيه الفاناديوم يسمى أمانيتا موسكاريا أو الذبابة الغارية.6 يحتويالفطر النموذجي على أقل من 0.5 ملغم من الفاناديوم كغم-1، ولكن يمكن أن يحتوي فطر أمانيتا موسكاريا على 100 ملغم من الفاناديوم كغم-1.6 أجزاءجسم الفطرالتي تحتوي على الفاناديوم هي الساق، وجلد الغطاء، ولحم الغطاء، والخياشيم، والجراثيم، والبصلة.6 يوجد أعلى تركيز للفاناديوم في البصلة عند 1000 ملغم من الفاناديوم في الكيلوجرام-1.6 يقعهذا الجزء من الفطر في الجزء السفلي من السديب، مما يجعله الأكثر عرضة للتلوث من التربة.6 عند النظر إلى التربة السطحية، كان متوسط الفاناديوم في التربة السطحية 60 ملجم كجم-1، مع نطاق يتراوح بين 1.28 و537 ملجم كجم-1.6 كان الفاناديوم الذيوجد في فطر المسكاريا سالب الشحنة وسمي أمافادين الشكل 3 من قبل باير وكنيفيل.6 اكتُشف من خلال التحليل الطيفي للرنين المغناطيسي الإلكتروني أن حالة أكسدة الفاناديوم كانت +4.6كما أشارت أطياف الرنين المغناطيسي الإلكتروني إلى أن الأجزاء المختلفة من الفطر تحتوي على نفس مركب أمافادين.6 وهما عبارة عنرابطين رباعي الأربطة الموضحة في الشكل 3 يمكنهما التنسيق مع مركز الفاناديوم، مما يخلق أيزومرين يظهران في خليط متساوٍ تقريبًا في الأمافادين الاصطناعي والطبيعي.6
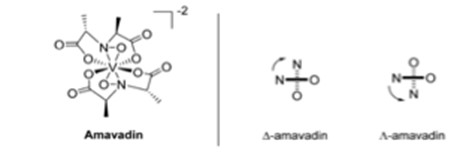
الشكل 3. هيكل الأمافادين، مع الأيزومرين D وL.6
إن أكسدة V(IV) إلى V(V) قابلة للانعكاس في الأمافادين، مما يعني أنه يمكن أن يكون له خصائص تحفيزية.6 تمالعثور على مجموعة واسعة من التفاعلات التي يحفزها المركب.6 أدى ذلك إلىتصنيع نظائر مختلفة للأمافادين بمراكز أيونات فلزية مختلفة أو روابط معدلة.6 وعندما تم تخليق الأمافادين من A. muscaria، وجد أن هناك معقدات مختلفة من الفاناديوم كان أبرزها أسيتات الفاناديل.6 حيثوجد أن المادة الصلبةتحتوي على 26% (وزن/وزن) من أسيتات الفاناديول و74% (وزن/وزن) من الأمافادين.6
الخلاصة
في الختام، ثبت أن للفاناديوم استخدامات متعددة في الأنظمة البيولوجية. بدءًا من علاج السرطان إلى الفطر. وقد بحثت الأبحاث في حالات الأكسدة المختلفة وكيفية اختزالها في الأنظمة البيولوجية، مثل الدم أو الخلايا. وحالات الأكسدة الأساسية للفاناديوم هي +3 و+4 و+5. كانت الروابط التي ارتبطت عادةً بالفاناديوم هي معقدات الأكسجين، وخاصةً الفانادات وأسيتات الفاناديل. لا يزال هناك المزيد من الأبحاث التي يجب إجراؤها على الفاناديوم وتأثيراته على المجتمع العلمي.
المراجع:
1. ج. كوستا بيسوا، مجلة الكيمياء الحيوية غير العضوية، 2015، 147، 4-24
2. A. Butler, and C. J. Carrano, Coordination Chemistry Reviews, 1991, 109, 61-65
3. D. Rehder، كيمياء الفاناديوم البيولوجي العضوي، وايلي، إنكوربوريتد، نيويورك، 2008.
4. X. Yang and K. Wang, in Progress in Molecular and Subcellular Biology, eds. W. E. G. Muller, P. Jeanteur, R. E. Rhoads, D. Ugarkovic, and M. R. Custodio. سبرينجر، مانز، ألمانيا، 2013، الفصل 1، ص 1-19.
5. D. Rehders, Metallomics, 2015, 7, 732
6. S. Braeuer, M. Walenta, L. Steiner, and W. Goessler, Royal Society of Chemistry, 2021, 36, 954-967.

 القضبان
القضبان
 الخرز والكرات
الخرز والكرات
 البراغي والصواميل
البراغي والصواميل
 البوتقات
البوتقات
 الأقراص
الأقراص
 الألياف والأقمشة
الألياف والأقمشة
 الأفلام
الأفلام
 فليك
فليك
 الرغاوي
الرغاوي
 رقائق معدنية
رقائق معدنية
 الحبيبات
الحبيبات
 أقراص العسل
أقراص العسل
 الحبر
الحبر
 صفائح
صفائح
 الكتل
الكتل
 التشابك
التشابك
 غشاء معدني
غشاء معدني
 اللوحة
اللوحة
 المساحيق
المساحيق
 قضيب
قضيب
 الصفائح
الصفائح
 البلورات المفردة
البلورات المفردة
 هدف الاخرق
هدف الاخرق
 الأنابيب
الأنابيب
 الغسالة
الغسالة
 الأسلاك
الأسلاك
 المحولات والآلات الحاسبة
المحولات والآلات الحاسبة
 Dr. Samuel R. Matthews
Dr. Samuel R. Matthews


